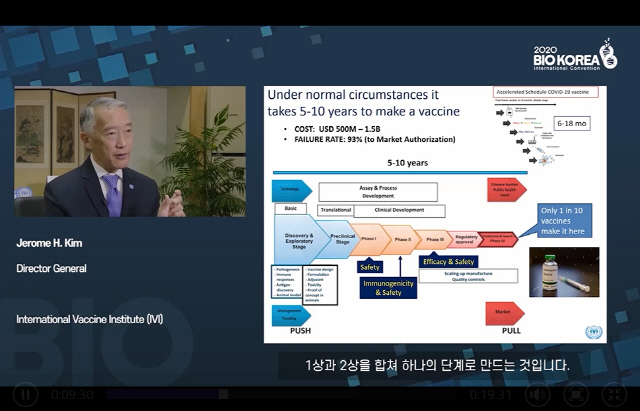
“보통 백신개발은 5년~10년 걸리지만 코로나19와 같은 특별한 상황인만큼 현재는 6~18개월 내로 목표를 세우고 있습니다.”(제롬 킴 국제백신연구소 사무총장)
올해 15회차를 맞은 아시아 최대 바이오 컨벤션 ‘바이오코리아 2020’가 18일 온라인 개막한 가운데 올해는 신종 코로나바이러스 감염증(코로나19)이 주요 화두로 떠올랐다.
제롬 킴 사무총장은 이날 특별 기조연설에서 “현재 전 세계에서 코로나19 백신 개발에 참여한 건수는 100개 이상이며 여기서 임상시험에 진입한 연구는 8건”이라면서 “1상과 2상을 합쳐 하나의 단계를 만드는 등 개발 기간을 단축할 수 있는데 기존 방식에 비해 효능과 안정성은 동일 하게 할 것”이라고 말했다.
이어 이어진 기업설명회에서 장신재 셀트리온 사장은 “현재 개발 중인 항체치료제는 감염된 환자의 바이러스를 즉각적으로 중화하는 효과를 낼 뿐 아니라 건강한 사람에 투여했을때 항체의 반감기인 2~3주정도 동안 외부에서 들어오는 바이러스를 막아낼 수도 있다”면서 “환자를 다루는 의료진, 긴급하게 (감염 위험이 높은) 업무를 수행해야 하는 사람에게 효과를 낼 수 있을 것”이라고 밝혔다. 이어 “항체 치료제는 화학 의약품과 비교해 부작용이 발생할 우려도 낮은 편”이라며 “예방 효과, 낮은 부작용 등 두 가지 장점을 바탕으로 개발하고 있다”고 설명했다.
국내 진단기업 최초로 미국 연방재난관리청(FEMA) 코로나19 관련 조달업체로 등록된 솔젠트도 유재형 대표가 나서 해외 수출 계획을 밝혔다. 유 대표는 자사 진단 키트에 대해 “현재 전 세계 54개국에 수출 중”이라며 “미국에서는 지난 4월 받은 공급허가에 그치지 않고 정식 허가를 받아 주정부 등과 장기 계약을 맺을 예정”이라고 말했다.
이밖에 김윤원 이뮨메드 대표는 “치료제 HzVSFv에 대한 임상 2상을 식약처에 신청해 2·4분기 내 영남대, 충남대, 계명대 등에서 시험을 시작할 것”이라며 “3·4분기엔 이탈리아에서도 임상을 진행할 예정”이라고 밝혔다. HzVSF는 이뮨메드가 당초 인플루엔자 치료제와 B형간염 치료제로 개발중이던 약물로 코로나19 발발 후 중증 코로나19 환자에 ’치료목적 사용 승인‘을 받아 사용 중이다. 치료목적 사용승인은 허가 제도와 별도로 치료수단이 없는 환자를 대상으로 한 만큼 상용화를 위해 임상시험을 별개로 진행해야 한다.
바이오코리아 2020은 18일부터 23일까지 6일간 진행된다. 코로나19 사태로 모든 행사를 온라인으로 진행하며 코로나19 특별세션 외에도 알츠하이머, 항체, 재생의료 등을 주제로 24개 세션으로 구성되며 국내외 93명의 연사가 참가한다.
/이주원기자 joowonmail@sedaily.com
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >