‘유전자 가위’로 불리는 유전자 편집 기술로 암세포의 유전자를 골라 죽일 수 있는 항암 기술이 국내에서 개발됐다.
울산과학기술원(UNIST)은 조승우 바이오메디컬공학과 교수와 기초과학연구원(IBS) 유전체항상성연구단 연구팀이 암세포의 디옥시리보핵산(DNA) 이중나선 중 한 가닥만 잘라도 암세포를 죽일 수 있는 유전자 편집 기술을 개발했다고 3일 밝혔다. 연구 성과는 미국암학회(AACR)가 발행하는 학술지 ‘캔서 리서치’에 이달 1일 게재됐다.
유전자 편집 기술 ‘크리스퍼(CRISPR)’는 2020년 노벨화학상 연구 성과로 선정됐으며 현재 학계에서 널리 쓰이고 있다. 암세포 역시 유전자를 가진 세포인 만큼 이 유전자를 조작해 효과적으로 죽이는 항암 기술이 연구돼왔다. 조 교수 연구팀은 2022년 관련 기술을 처음 제시했지만 암세포가 치명상을 입으려면 20개가 넘는 가위를 한꺼번에 동원해야 했다. 유전자 가위를 암세포까지 전달하기가 까다롭고 정상적인 부위까지 손상시킬 위험이 있었다.
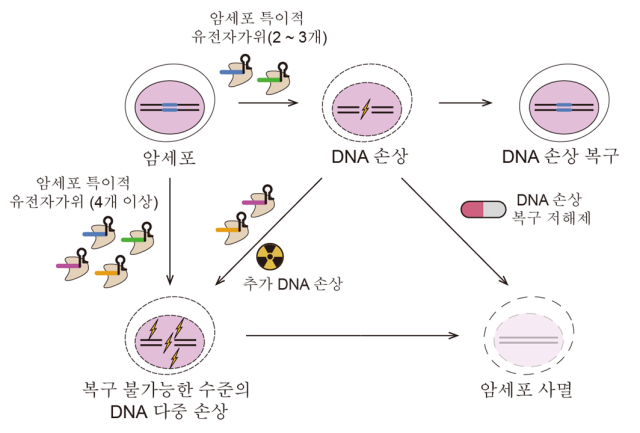
연구팀은 기술을 개선해 암세포의 유전자 정보를 담은 DAN 이중나선 가닥들 중 한 가닥만 잘라도 사멸 효과를 보는 데 성공했다. 유전자 가위도 4개만 동원하면 된다. 가닥이 절단되면 이를 자연적으로 수선하는 ‘PARP 단백질’을 억제하는 물질을 함께 사용해 절단을 쉽게 만든 것이다. PARP 단백질 억제제는 또 기존에도 일부 유전자 변이로 발병하는 암 치료 효과를 가졌는데 유전자 가위와 함께 사용되면 보다 다양한 암에 대응할 수 있다는 게 연구팀의 설명이다.
연구팀은 실제 유전자 가위와 PARP 억제제를 대장암 환자 암세포로 만든 오가노이드(장기 모형) 조직에 투여하자 성장이 억제되는 것을 확인했다. 대장암 세포를 생쥐에 이식해 진행한 전임상 실험에서도 6주 동안 종양 크기가 절반 이하로 줄어들었다.
조 교수는 “가위 전달 과정의 복잡성과 세포 독성을 크게 줄여 임상 적용 가능성을 높인 연구이자 표적 항암제인 PARP 억제제의 적용 범위를 넓힌 결과”라며 “다른 표적 항암제나 방사선 치료와 병행했을 때 시너지 효과를 보여 단독 요법뿐 아니라 병용 치료 전략으로도 이어질 수 있을 것으로 기대된다”고 말했다.
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >








 sookim@sedaily.com
sookim@sedaily.com







































