국내외 연구진이 2곳 이상에 자리잡은 교모세포종(악성 뇌종양)을 치료할 맞춤형 ‘전천후 표적항암제’를 골라내는 방법론을 함께 개발했다.
삼성서울병원 난치암연구사업단 남도현(신경외과)·박웅양(삼성유전체연구소장) 교수팀은 미국 콜롬비아대 라울 라바단 교수팀과 협력해 이 같은 성과를 거뒀다. 연구논문은 저명 국제학술지 ‘네이처 제네틱스’ 4월 1일자에 실릴 예정이며 이에 앞서 7일 오전 1시(한국시간) 온라인으로 발표됐다.
연구팀이 국내 교모세포종 환자 52명의 둘 이상 종양 부위에서 떼낸 조직들을 비교분석해보니 서로 근접해 있는 종양, 가까운 곳에서 재발한 종양은 유전체 발현·변이 양상이 비슷했다. 반면 멀리 떨어져 있거나 변이·진화 단계가 다른 종양들의 유전체 구조는 적잖은 차이가 났다.
그래서 공통분모, 특히 암 발생·증식 초기 단계부터 전이·재발에 이르기까지 지속적으로 관여하는 ‘뿌리급 유전자’를 가려냈다. 의료영상, 유전체 분석 결과와 수학적 모델링 기법을 활용해 암 특이적 유전자들이 나무의 뿌리-줄기-가지-잎 중 어디에 해당하는 지 분류했다. 이어 환자의 종양 세포에 뿌리 유전자의 활성을 억제하는 표적항암제들을 처리해 반응성이 좋은 것을 골라냈다. 2곳 이상에 자리잡은 교모세포종을 억제·퇴치할 수 있을 것으로 기대되는 ‘전천후 표적항암제’다.
지금까지는 1개 종양 부위의 유전자 변이만 확인하고 표적항암제를 선정하는 경우가 많아 항암치료 효과가 거의 없었다.
논문의 제1저자인 이진구 삼성서울병원 난치암연구사업단 연구원은 “서로 떨어져 있는 종양에 각각 100개가 넘는 암 특이적 돌연변이가 발견되는 환자의 경우 대개 10개 안팎의 뿌리급 변이 유전자를 골라낼 수 있다”며 “환자의 종양 세포에 여러 표적항암제들을 반응시켜 결과가 좋은 것을 골라내면 실제 항암치료에서 효과를 볼 가능성이 있다”고 말했다.
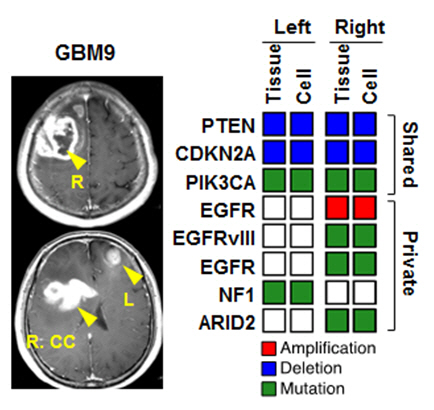
연구팀은 또 PIK3CA 유전자의 돌연변이가 멀리 떨어진 두 종양의 발생에 공통적으로 관련돼 있음을 규명했다. 이를 표적으로 하는 PI3K 억제 약물의 임상 적용 가능성도 환자의 세포에서 확인했다. PIK3CA 유전자의 변이는 대장 직장암·위암·교모세포종에선 약 30%, 유방암·폐암에선 그보다 낮은 빈도로 나타나는 것으로 알려져 있다.
/임웅재기자 jaelim@sedaily.com
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >