|
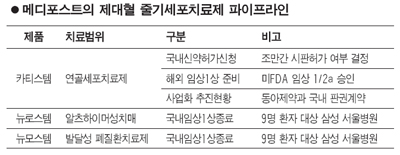
줄기세포 치료제로 치매 뿌리 뽑는다 메디포스트 임상1상 마치고 개발 본격화… 폐질환 치료제도 병행이런 꿈같은 일이… 치매 완치 길 열리나 황정원기자 garden@sed.co.kr 알츠하이머성 치매 줄기세포 치료제 임상 1상이 사실상 종료돼 개발이 본격화될 전망이다. 지금까지 전세계적으로 치매 관련 의약품은 증상 완화에 일부 효과가 있을 뿐 근본적인 치료제가 없어 줄기세포 치료제에 대한 기대가 크다. 27일 식품의약품안전청과 관련업계에 따르면 메디포스트는 최근 개발 중인 알츠하이머성 치매 치료제 '뉴로스템-AD'와 폐질환 치료제 '뉴모스템' 등 줄기세포 치료제 2종의 제1상 임상시험 피험자 투여를 완료하고 식약청에 종료 보고서를 제출했다. 약 2~3달 안에 최종 임상 결과 분석을 완료해 식약청에 제출하면 공식적으로 임상 1상이 종료된다. 업계에서는 이르면 내년 상반기 중에 임상 2상에 돌입할 것으로 내다보고 있다. 이들 두 치료제는 모두 제대혈에서 분리ㆍ배양한 줄기세포를 이용한 것이다. 제대혈 성체줄기세포치료제는 동종세포이식이 가능하기 때문에 원가경쟁력과 대중화 측면에서 우위를 확보, 상업화할 경우 시장성이 높다. 양윤선 메디포스트 대표는 "사람을 대상으로 임상 1상을 마친 것은 구체적으로 희망을 검증한 것"이라며 "연골재생 치료제 '카티스템'의 임상 경험이 있어 다음 절차는 신속하게 진행해 나갈 수 있을 것"이라고 밝혔다. 카티스템의 임상 시험이 약 5년10개월 걸렸다면 두 치료제는 그 기간이 상당수 단축될 것임을 의미한다. 메디포스트는 '뉴로스템-AD'에 대해 지난해 11월 식약청으로부터 임상시험 승인을 획득한 이후, 올 3월부터 9명의 환자군을 대상으로 안전성과 잠재적 치료 효과 등을 추적 관찰해 왔다. '뉴로스템-AD'는 아밀로이드 베타 단백질을 줄이고 뇌신경세포의 사멸을 억제하며, 뇌 내의 신경전구세포를 일반 신경세포로 분화할 수 있도록 돕는 역할을 하게 된다. 알츠하이머성 치매의 원인 물질 감소뿐 아니라 신경 재생과 같은 근본 치료도 가능할 것으로 기대된다. 이와 관련 알츠하이머성 치매 관련 시장은 전세계적으로 700조원, 국내는 6,500억원 규모에 이른다. 화이자제약이 임상 3상에서 실패하는 등 기존 제약업계에서 뚜렷한 치료제를 내놓고 있지 못한 상황이어서 줄기세포를 이용한 치료제에 대한 기대가 크다. 이와 함께 메디포스트는 지난해 7월 임상시험 승인을 받고 올해 2월부터 9명의 피험자를 대상으로 진행한 미숙아의 기관지폐이형성증 예방치료를 목적으로 하는 치료제인 '뉴모스템'도 피험자 투여를 완료했다. '뉴모스템'은 폐조직 재생과 염증소견 개선 효과가 기대되는 제품이다. 한편 메디포스트는 연골재생 치료제 '카티스템'이 조만간 식약청의 품목허가를 받으면 2번째로 줄기세포 치료제 상업판매에 돌입하게 된다. 김지현 키움증권 연구원은 "뉴로스템과 뉴모스템은 실질적인 경쟁자가 없어 회사의 펀더멘털을 바꿀 수 있을 정도"라며 "카티스템으로 안타를 치고(시장에서 검증을 받고) 두 제품으로 홈런(상업판매 성공)을 기대하는 것 같다"고 말했다.
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >