건국대학교 오덕근 교수 연구팀이 미생물에 존재하는 효소를 이용하여 인체 내 존재하는 지질 조절제와 유사한 물질들을 개발하였다. 부작용 적은 치료제 개발의 가능성이 열렸다.
당뇨병은 인슐린 분비 및 기능의 문제로 생기는 난치성 대사질환이다. 최근 30대 이상 성인의 10명 중 3명이 당뇨병 또는 고위험 군으로 보고되면서 이에 대한 우려가 높아지고 있다. 현재 사용되는 당뇨병 치료제는 강력한 효과에 비해 심부전 발병 및 체중 증가 등의 부작용을 동반하고 있어, 대체 치료제의 개발이 시급한 실정이다.
연구팀은 부작용이 적은 당뇨병 치료를 위하여 천연 물질의 발굴에 주목, 일부 미생물로부터 인간 유래 지질조절제인 헤폭실린, 트리오실린 등의 물질들을 합성해냈다. 또한 세균에서 지질 조절제의 생합성에 관여하는 효소와 그 대사 경로도 규명했다. 인간 체내에서 지질 조절제를 합성하는 지방산화효소, 수산화지방산 형성효소와 같은 기능을 가지는 유사 단백질을 미생물에서 발견했고, 이를 활용하여 다양한 지질 조절제를 생합성했다.
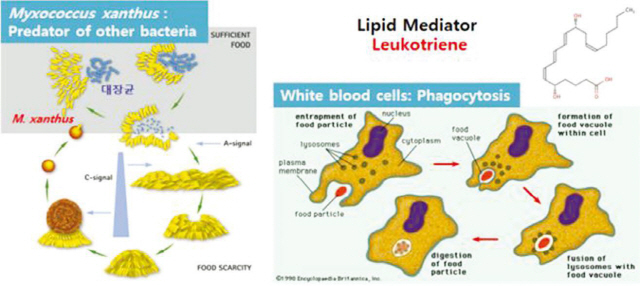
▲ 대장균을 포식하는 믹소코쿠스 잔투스와 세균 을 포식하는 백혈구
백혈구가 생산하는 지질조절제는 루코트리엔임을 알고 믹소코쿠스 잔투스가 생산하는 지질조절제를 조사한 결과 헤폭실린과 트리오실린임을 규명하였다.
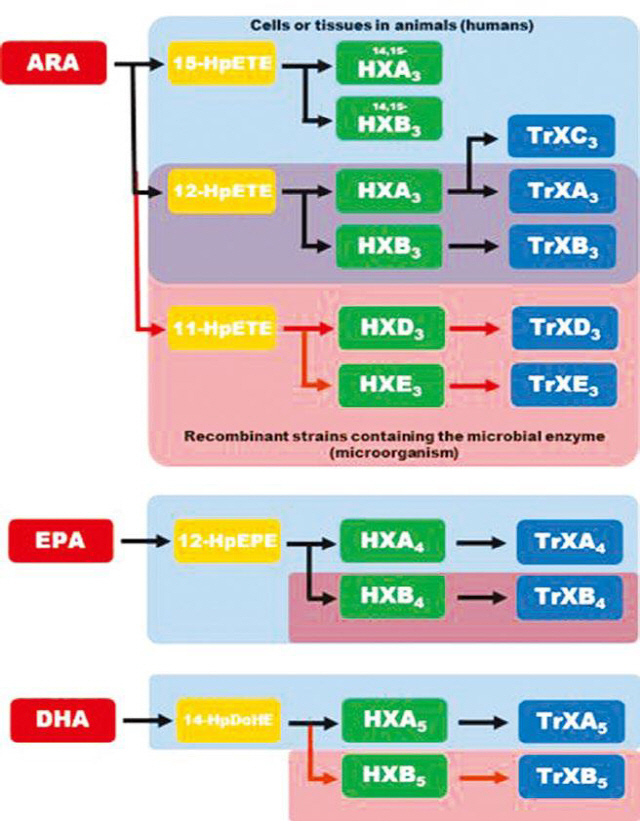
▲ 현재까지 확인된 헤폭실린과 트리오실린 및 그 유사체
현재까지 보고된 헤폭실린과 트리오실린의 합성 경로이다. 파란색 상자로 표시된 물질은 인간을 비롯한 포유류 내에서 생성되어 현재까지 보고된 헤폭실린과 트리오실린을 나타낸 것이고, 빨간색 상자로 표시된 물질은 본 연구를 통해 미생물 효소들을 이용해 생합성된 헤폭실린과 트리오실린을 나타낸 것이다.
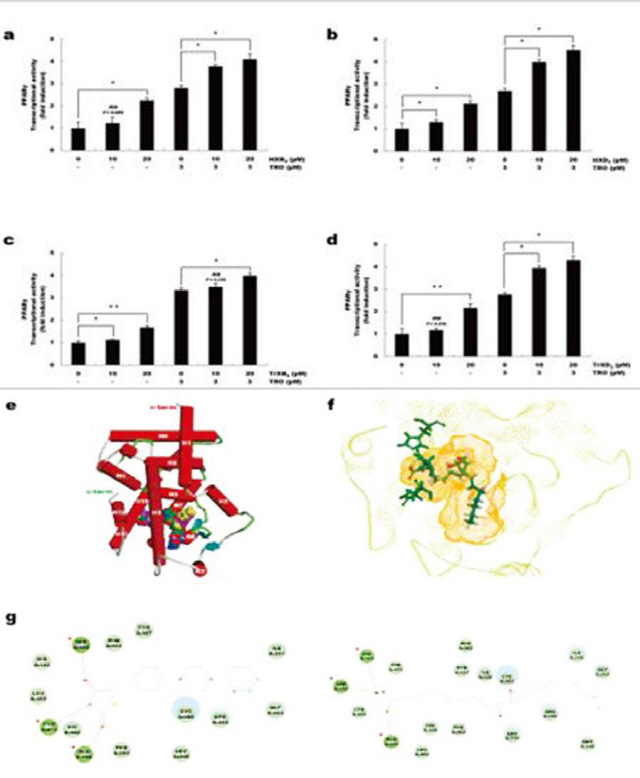
▲ 미생물 지방산화효소로 전환된 헤폭실린이 PPARγ 활성이 미치는 영향
믹소코쿠스 잔투스 유래 지방산화효소로 전환된 헤폭실린류와 트리오실린류가 PPARγ 활성에 미치는 영향을 조사하였다. (a-d) 각각 헤폭실린 B3, 헤폭실린 D3, 트리오실린 B3, 그리고 트리오실린 D3가 PPARγ의 활성에 미치는 영향을 확인하였다. 단독적으로 처리하였을 때는 기존의 작용제로 알려진 트로글리타존(Troglitazone)보다 활성을 낮지만 PPARγ의 전사활성을 증가시키는 것으로 나타났으며, 트로글리타존과 혼합 처리 시에도 효과적으로 증가시키는 것을 확인하였다. (e) PPARγ의 수용체 결합부위(receptor binding domain)에 hepoxilin과 trioxilin이 결합되어 있는 모델링 구조를 컴퓨터 분석을 통해 나타내었다. (f) 헤폭실린 B3가 PPARγ의 수용체 결합부위에 결합했을 때, 확인되는 결합 포즈와 상호작용을 가지는 잔기를 나타내었다. (g) 기존의 PPARγ의 작용제로 알려져 있는 치아졸리딘디온계의 로지글리타존(rosiglitazone)과의 상호작용 잔기 비교를 하였다. 왼쪽은 로지글리타존이 PPARγ의 수용체 결합부위의 특정 아미노산인 GLN286, SER289, TYR473과 상호작용을 가지는 것을 보여주며, 오른쪽은 헤폭실린 B3가 PPARγ의 수용체 결합부위의 특정 아미노산인 GLN286, SER289, HIS323과 결합하고 있음을 보여준다.
서울경제 파퓰러사이언스 편집부 / 정승호 기자 saint096@naver.com
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >