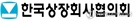의약품 성분이 뒤바뀌어 품목허가가 취소된 코오롱생명과학의 골관절염 유전자 치료제 ‘인보사케이주’(이하 인보사)와 관련한 부작용 보고 사례가 300건이 넘는 것으로 나타났음에도 식품의약품안전처의 역학조사가 이루어지지 않은 것으로 나타났다.
국회 보건복지위원회 정춘숙 의원이 4일 식약처에서 받은 자료에 따르면, 지난 2014년 1월 1일부터 지난 8월 11일까지 인보사와 관련해 총 329건의 신고가 한국의약품안전관리원에 접수됐다. 이 가운데 종양 관련 부작용 보고 건수는 8건이었다. 종양 관련 보고내용은 악성 자궁내막 신생물(2건), 위 암종(2건), 췌장암, 간 신생물, 여성 악성 유방 신생물, 이차 암종 등이었다. ‘효과 없는 약’이라고 부작용을 보고한 사례도 총 63건(19.1%)에 달했다. 다른 무릎 주사제의 경우 약효가 없다는 부작용 보고 비율이 10.7%에 그치는 점과 비교해 2배 가까이 높았다.
하지만 식약처는 이 같은 이상 사례 보고에도 ‘약물과의 관련성 없음’ 또는 ‘공란처리’로 등록하며 역학조사를 하지 않고 있었다. 특히 종양 관련 이상 사례 8건에 대해서도 ‘평가 불가’, ‘평가 불능’, ‘평가 곤란’으로 보고받았던 것으로 알려졌다. 정 의원은 “사태가 이렇게 심각한데, 식약처가 국민의 안전과 관련한 사안을 너무 안이하게 처리하는 게 아니냐”고 질타했다.
인보사는 주성분 중 하나가 허가 당시 제출한 자료에 기재된 연골세포가 아닌 종양 유발 가능성이 있는 신장 세포(293유래세포)로 드러나 논란을 일으켰다. 식약처는 이에 따라 3월 31일 중앙약사심의위원회를 열어 코오롱생명과학에 자발적으로 인보사의 제조·판매 중지하도록 조처를 내렸다. 이후 식약처는 5월 28일 인보사의 품목허가를 취소하겠다고 발표했고, 7월 3일 취소 처분을 확정했다. 식약처는 3천여명으로 추정되는 인보사 투여 환자를 대상으로 이상 반응 장기추적조사 시스템 등록을 마친 뒤, 15년간의 장기 추적조사에 돌입해 암 같은 이상 반응과 인보사와의 인과관계를 확인할 계획이다. 인보사는 2017년 7월 식약처 허가 후 의약품 성분 논란으로 유통·판매가 중지된 지난 3월 31일까지 438개 병·의원에서 3,707건 투여됐다. 식약처는 무릎 양쪽에 주사하는 경우 등을 고려해 최대 투여환자를 3,014명으로 추정하고 있다.
/우영탁기자 tak@sedaily.com
< 저작권자 ⓒ 서울경제, 무단 전재 및 재배포 금지 >








 tak@sedaily.com
tak@sedaily.com